Benessere
Probiotici, depressione e ansia – Come i probiotici cambiano il modo in cui ti senti

Conosciamo tutti l’espressione “una sensazione di pancia” ad indicare qualcosa di naturalmente istintivo e legato al pensiero; tuttavia, le ultime ricerche mostrano che è ben più di un modo di dire, e che in realtà si tratta di qualcosa di molto reale. Questo perché il nostro intestino è letteralmente un “secondo cervello”, con il suo sistema nervoso – il sistema nervoso enterico o SNE, che consiste di milioni di neuroni, e una superstrada di agenti chimici e ormoni che forniscono un flusso costante di informazioni tra il cervello e l’intestino stesso. In questo articolo, analizzeremo le ultime ricerche relative al collegamento tra i batteri intestinali, i probiotici, la depressione e l’ansia.
Table of Contents
Probiotici, depressione e ansia
Oggi sappiamo che le informazioni passate attraverso il nostro sistema nervoso enterico, oltre agli ormoni e agli agenti chimici intestinali verso il cervello, sono direttamente collegate ai 40 trilioni di batteri che qui vivono. Le ricerche mostrano inoltre che ci sono differenze significative nei batteri intestinali tra chi soffre di depressione e altre malattie mentali rispetto a chi non ne soffre. Queste nuove conoscenze hanno creato un modo di vedere le patologie mentali completamente nuovo. La connessione tra l’intestino e il cervello è stata segnalata inizialmente più di 100 anni fa da Elie Metchnikoff, uno scienziato francese vincitore del premio Nobel diventato famoso per aver bevuto di proposito acqua contenente il batterio del colera, riuscendo a sopravvivere. Egli lo fece per provare ciò in cui credeva, dimostrando che la forza del sistema immunitario era diversa da persona a persona, e che ciò che rendeva infetta una persona potrebbe non aver infettato un’altra.
La connessione tra il cervello e i batteri intestinali
Metchnikoff credeva inoltre che tutte le parti del corpo fossero collegate, e che le cure mediche avrebbero dovuto guardare al corpo come una struttura unica anziché trattare i sintomi solo nell’area in cui era localizzato il problema. Secondo lui il rafforzamento dei batteri intestinali con l’assunzione di cibi fermentati avrebbe potuto migliorare tutti i sistemi del corpo, oltre che tenere alla larga la demenza e la degenerazione cerebrale legate all’invecchiamento. I suoi lavori gli consentono a pieno titolo di essere considerato la prima persona nella storia ad aver sviluppato il concetto di probiotici.

Tuttavia, le sue argomentazioni su un approccio che comprendesse attenzione verso tutto il corpo nella medicina persero popolarità dopo la sua morte, e per i successivi 80 anni la scienza medica si è concentrata sulla specializzazione, dove i medici lavoravano per comparti stagni cercando di non sovrapporre le aree di competenza. Ad esempio, un gastroenterologo si sarebbe concentrato solo sul tratto gastrointestinale e sul fegato, mentre un neuroscienziato avrebbe mirato la sua attenzione solo sul cervello senza che nessuno dei due specialisti si fosse preoccupato di come un sistema avrebbe potuto influire sull’altro. Tutto ciò ha portato alla creazione di un programma di cure dall’alto verso il basso per le patologie mentali, dove le moderne cure farmaceutiche come gli antidepressivi o le benzodiazepine (tranquillanti) si concentravano esclusivamente sul cervello.
Uno studio: la connessione tra probiotici, depressione e ansia
Tuttavia, in anni più recenti l’attenzione dei ricercatori è iniziata a cambiare, dopo che alcuni studi hanno riscontrato un chiaro collegamento tra i batteri intestinali e depressione e ansia. In uno studio sui topi, i ricercatori canadesi della McMaster University hanno scoperto che potevano renderli nervosi o calmi, o felici e depressi, in base a farmaci antibiotici che somministravano loro e che alteravano la loro flora intestinale (conosciuta anche come microbioma). A questo punto ci si potrebbe chiedere: come si fa a sapere quando un topo è depresso? In realtà la questione non è così ridicola come si potrebbe inizialmente pensare. In realtà i topi hanno molti tratti genetici in comune con l’uomo, e presentano inoltre somiglianze comportamentali, ad esempio nel fatto di essere animali socievoli e curiosi. Ai topi piace vivere con altri tipo, perciò risulta molto evidente quando non lo fanno, o quando il loro comportamento sociale cambia. E’ proprio come negli esseri umani, dove la depressione è spesso associata al ritiro dalla vita sociale da parte di chi ne è affetto: i topi fanno altrettanto. I ricercatori possono inoltre giudicare i livelli di ansietà presentando ai topi dei nuovi compagni, giochi o aree da esplorare verificando in quanto tempo riescano a completare nuovi compiti. In ragione di tutto ciò, è stato semplice per i ricercatori scoprire quanto la modifica dei microbiomi dei topi ne modificava il comportamento. Ulteriori esperimenti alla McMaster University hanno riguardato l’ansia nello specifico, per mezzo dell’osservazione di topi che erano stati allevati geneticamente in modo che avessero tratti di timidezza o di avventurosità. I ricercatori hanno trapiantato il microbioma dai topi avventurosi a quelli timidi e hanno scoperto che nel corso del tempo i topi timidi potevano diventare più sicuri di sé1.
Batteri cattivi e depressione
I ricercatori hanno anche fatto riferimenti incrociati tra queste osservazioni comportamentali e test di laboratorio. Essi hanno aumentato il numero dei batteri cattivi nel tratto digerente dei topi e li hanno sottoposti a test, scoprendo la diminuzione dei livelli di un ormone chiamato BDNF, che è sostanzialmente un ormone della crescita per il cervello, oltre che la diminuzione della quantità di 5-HT, che sono recettori della serotonina nel cervello. I test hanno portato a questi risultati a seguito della modifica del microbioma dei topi, che sono risultati meno portati a sviluppare nuove cellule cerebrali, e inoltre meno capaci di sentire gli effetti della serotonina, neurotrasmettitore della “felicità”. La ricerca ha coniato una nuova espressione – il cosiddetto “asse intestino-cervello” – una linea immaginaria tra il cervello e l’intestino che ha un impatto biologico molto reale.

I probiotici e la depressione – Come funziona l’asse intestino-cervello?
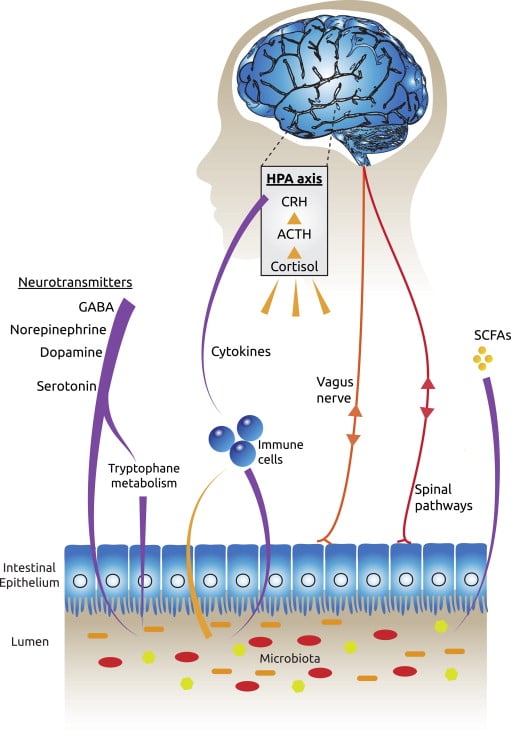
Normalmente l’intestino e il cervello si mantengono su un giusto mezzo, tuttavia, quando si verificano degli sbilanciamenti e il corpo finisce sotto stress, l’intestino e il cervello possono a loro volta perdere l’equilibrio. Questo stress può verificarsi sotto molteplici forme. Lo stress psicologico si trova ovunque nel nostro frenetico mondo. Pressioni finanziarie, lavorative, eventi traumatici nella vita di ciascuno e altri stress hanno un impatto molto significativo sul corpo e possono modificare anche i nostri batteri intestinali. Anche i vari tipi di stress fisiologico rappresentano una reale minaccia per l’intestino. L’inquinamento, i regimi alimentari non naturali e composti da cibi industriali e la mancanza di cibi fermentati che sarebbero stati parte naturale della dieta per tutta la nostra evoluzione, i trattamenti antibiotici, i pesticidi, le sostanze chimiche e altri medicinali, oltre che fumo e alcol possono tutti avere un effetto negativo sul nostro intestino. Persino lo stress di cui soffre una donna incinta può venire trasferito al bambino e influenzarne il microbioma2 3, come spiega la dottoressa Natasha Campbell Mcbride, autrice del libro “Gut and Psychology Syndrome”: “Il bambino acquisisce la sua flora intestinale al momento della nascita, quando il neonato passa attraverso il canale uterino della madre. Perciò, qualsiasi cosa viva nel canale uterino e nella vagina della madre, diventa la flora intestinale del bambino. Cosa vive nella vagina della madre? Si tratta di un’area densamente abitata del corpo di una donna. La flora vaginale viene dall’intestino. Perciò, se la madre ha una flora intestinale anomala, avrà le stesse anomalie nel proprio canale uterino.” Perciò lo stress produce cambiamenti nella flora intestinale, e ogniqualvolta questo accade, vi sono reazioni nel corpo che vengono trasferite al cervello e che cambiano il modo in cui ci sentiamo.
Tre percorsi principali che cambiano nel segnale intestinale al cervello
1 – I batteri intestinali e il sistema immunitario
Il primo modo in cui i batteri intestinali possono causare problemi al cervello è attraverso la produzione di infiammazione nel nostro corpo. Questa infiammazione è causata dall’attivazione del sistema immunitario, il quale cerca di proteggerci da ciò che riconosce come una minaccia. Nel breve periodo, questa attivazione ha ruoli benefici, ad esempio serve a combattere le infezioni o a guarire le ferite, come quando una caviglia si gonfia dopo una storta. Tuttavia, troppi batteri cattivi possono determinare questa attivazione del sistema immunitario sul lungo periodo o farla diventare cronica, il che può causare danni in tutto il corpo. Oggi gli studi scientifici sono concordi nel confermare che questa attivazione può causare depressione e ansia4 5. L’attivazione del sistema immunitario produce molecole chiamate chitocine, le quali inducono altre cellule a produrre una risposta infiammatoria . Ad esempio, quando le chitocine inviano segnali al cervello, esso può rispondere producendo ormoni dello stress come il cortisolo.

Il sistema immunitario può anche essere attivato nella produzione di infiammazioni quando le modifiche al microbioma fanno sì che l’epitelio intestinale (la barriera tra intestino e il resto del corpo) diventi pieno di piccole perforazioni o aperture (fenomeno conosciuto come permeabilità intestinale).
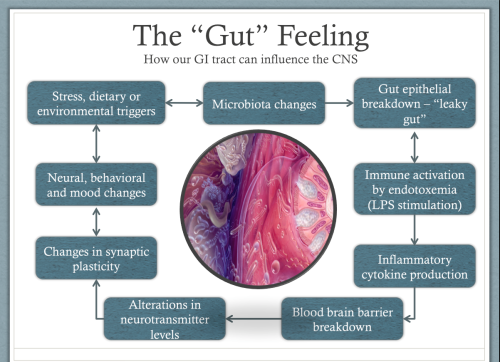
Ciò può permettere a molecole tossiche chiamate lipopolisaccaridi (LPS) di penetrare attraverso le pareti intestinali. Queste molecole LPS vivono nelle membrane cellulari dei nostri batteri intestinali e vengono rilasciate quando essi muoiono. Di solito esse abbandonano il corpo in sicurezza attraverso il nostro intestino quando espelliamo le feci. Tuttavia, quando la permeabilità intestinale consente ad esse di penetrare nel nostro corpo, ciò determina una forte risposta infiammatoria da parte del sistema immunitario. Se le modifiche nella flora intestinale sono consistenti, l’infiammazione può anche determinare modifiche nella barriera emato-encefalica. La barriera emato-encefalica è la membrana che separa il sangue dai fluidi cerebrali. Normalmente, la barriera consente il passaggio di poche molecole selezionate, ma l’infiammazione può farla diventare più permeabile consentendo così l’ingresso a molecule che non dovrebbero trovarsi in quel luogo, e che possono essere nocive per le cellule cerebrali. Ciò può impedire al nostro cervello di realizzare nuove connessioni neurali, con conseguenti difficoltà nell’apprendimento e nello sviluppo, lasciandoci intrappolati in schemi comportamentali negativi6.
2 – I batteri intestinali e il nervo vago
Il secondo modo in cui il nostro intestino può influire sul nostro cervello è attraverso il nervo vago. Il nervo vago è il nervo più lungo del corpo, che parte dal cranio e scende fino all’intestino, controllando il cuore, i polmoni e il tratto digerente. Quando si verifica uno squilibrio nel nostro intestino, il nervo vago può segnalarlo al cervello e causare una risposta infiammatoria. Esso può anche far sì che il cervello rilascio ormoni dello stress nel corpo e all’interno del cervello stesso. Questi ormoni possono influire su aree del cervello responsabili dell’assunzione di decisioni, della rabbia e della paura, come la corteccia prefrontale e il sistema limbico. Il nervo vago ha inoltre recettori per le chitocine prodotte dal sistema immunitario e rappresenta un altro percorso attraverso il quale le infiammazioni nel corpo vengono segnalate al cervello.
3 – Neurotrasmettitori e batteri intestinali
Il percorso del nervo vago all’interno del corpo
L’ultimo modo in cui l’intestino può influire sul modo in cui ci sentiamo è attraverso la produzione di neurotrasmettitori. I batteri intestinali producono alcuni neurotrasmettitori, tra cui la serotonina, i recettori GABA, la dopamina e la norepinefrina. L’80-90% della serotonina presente nel corpo è prodotto dall’intestino, e la serotonina è l’agente chimico responsabile della sensazione di benessere e il neurotrasmettitore è un bersaglio per gli antidepressivi SSRI (Inibitori selettivi della ricaptazione della serotonina).
Il neurotrasmettitore GABA è il nostro rilassante naturale, quello che ci fa rilassare. La dopamina ci dà motivazione, ciò che ci spinge ad alzarci dal letto la mattina, oltre che la capacità di provare piacere e gratificazione, come quando ci si siede davanti al proprio piatto preferito, o dopo aver ricevuto un aumento di stipendio. D’altro canto, la norepinefrina stimola la risposta “fuggi o lotta” o lo stress. Perciò quando problemi di varia natura nel nostro intestino influiscono su questi neurotrasmettitori aumentandone o diminuendone la produzione, possono verificarsi potenti effetti sulla nostra salute mentale.
Probiotici per la depressione e probiotici per l’ansia
Le buone notizie sono che le ultime ricerche dimostrano che queste modifiche nei batteri intestinali causate dallo stress, e che la reazione del corpo a tali modifiche, possono essere annullate con probiotici o con cibi fermentati. La ricerca sugli esseri umani è ancora agli inizi, e con gli uomini gli scienziati non hanno la stessa libertà che hanno con i tipo, e non è possibile generare geneticamente un essere umano affinché abbia determinati batteri intestinali. Tuttavia, gli studi iniziali hanno prodotto risultati entusiasmanti. Ad esempio, uno studio pubblicato a marzo dell’anno scorso sulla rivista Nutrition ha esaminato pazienti affetti da DDM (disturbo depressivo maggiore). I ricercatori hanno somministrato a metà dei partecipanti allo studio dei probiotici, e all’altra metà un placebo, e hanno misurato i punteggi di depressione dopo un periodo di 8 settimane, oltre che i livelli di insulina e di infiammazione (misurati con un marker del sangue chiamato proteina C-reattiva). Essi hanno scoperto che dopo il periodo di 8 settimane chi aveva assunto i probiotici aveva dei punteggi di depressione significativamente ridotti, oltre che livelli di insulina inferiori e meno infiammazioni nel corpo rispetto al gruppo che aveva assunto il farmaco placebo7. Dei ricercatori olandesi hanno inoltre suggerito che i probiotici per bambini possono aiutare a correggere il danno patito dalla loro flora intestinale al momento della nascita da madri con elevati livelli di stress durante la gravidanza8. Uno studio precedente del 2011 pubblicato sulla rivista dal meraviglioso nome Gut Microbes (“microbi intestinali”) ha rilevato che l’assunzione di probiotici per sole 2 settimane può ridurre i sintomi della depressione e dell’ansia, oltre che ridurre i livelli del cortisolo, l’ormone dello stress9. Inoltre, uno studio del 2015 del College of William and Mary pubblicato nella rivista Psychiatry Research ha investigato sugli schemi alimentari di 700 studenti, scoprendo che coloro che mangiavano più cibi fermentati avevano meno problemi legati all’ansia10.
Quali sono i migliori probiotici per la depressione e i migliori probiotici per l’ansia?
Dal momento che la ricerca sta mostrando risultati molto incoraggianti, è ancora più importante scegliere un probiotico di alta qualità. Non tutti i probiotici sono uguali, e sul mercato esistono molte marche di bassa qualità. Cerca probiotici potenti (con 50 miliardi di UFC per compressa), multiceppo, con almeno 5 miliardi di UFC per ceppo (in modo che 10 ceppi diano un totale di 50 miliardi di UFC per compressa). E’ inoltre molto importante trovare aziende produttrici di probiotici che utilizzino ceppi brevettati, resistenti agli acidi e al calore, in modo che non muoiano nella confezione o nello stomaco prima di raggiungere l’intestino. Ciò significa cercare un numero elencato immediatamente dopo il ceppo. Ad esempio, il Bifidobacterium longum BI-05. La parte “BI-05” indica il ceppo specifico. Se non c’è un numero dopo il ceppo, ciò significa che l’azienda sta verosimilmente utilizzando ceppi economici e generici senza benefici provati sulla salute fisica e mentale, che dovrebbero essere evitati. Le aziende che suggeriscono di conservare i loro probiotici in frigorifero dovrebbero far suonare un altro campanello d’allarme. I ceppi di probiotici brevettati e resistenti al calore non richiedono una cosa del genere, e durante la permanenza delle confezioni in magazzino e nel periodo del trasporto i probiotici non vengono tenuti in celle frigorifere, perciò è molto probabile che molti batteri saranno già morti quando la confezione sarà consegnata a casa tua. Inoltre, cerca probiotici che contengano prebiotici (che sono il cibo dei probiotici, per assicurare che ancora più batteri “buoni” raggiungano vivi il tuo intestino).
💬 Hai qualche idea? Condividila nei commenti. Siamo sempre felici di conoscere il pensiero di menti curiose.
📩 E intanto che sei qui, iscriviti alla nostra newsletter per altre idee intelligenti (e consigli segreti)!
Riferimenti:
- Premysl Bercik, Emmanuel Denou, Josh Collins, Wendy Jackson, Jun Lu, Jennifer Jury, Yikang Deng, Patricia Blennerhassett, Joseph Macri, Kathy D. McCoy, Elena F. Verdu, Stephen M. Collins, The Intestinal Microbiota Affect Central Levels of Brain-Derived Neurotropic Factor and Behavior in Mice, Gastroenterology, agosto 2011,Volume 141, Numero 2, Pagine 599–609.e3 ↩︎
- Zijlmans M, Korpela K & Riksen-Walraven JM (2015). Maternal prenatal stress is associated with the infant’s intestinal microbiota.Psychoneuroendocrinology. 53:233-45. ↩︎
- John Cryan (University College Cork, Ireland), How Bacteria Can Cause Mood and Psychotic Disorders?”. GUT BRAIN SYMPOSIUM 2016. https://www.youtube.com/watch?v=hxUsoQqKVg4 ↩︎
- Miller AH, Raison CL. The role of inflammation in depression: from evolutionary imperative to modern treatment target. Nat Rev Immunol. 2016;16:22–34. Questo studio delinea le attuali prove relative alle infiammazioni nell’eziologia e nella patofisiologia della depressione e un’analisi ragionata per approcci antinfiammatori e immunoregolatori per il trattamento della depressione. ↩︎
- Braniste V, Al-Asmakh M, Kowal C, Anuar F, Abbaspour A, Tóth M, Korecka A, Bakocevic N, Ng LG, Kundu P, Gulyás B, Halldin C, Hultenby K, Nilsson H, Hebert H, Volpe BT, Diamond B, Pettersson S11. The gut microbiota influences blood-brain barrier permeability in mice. Sci Transl Med. 19 novembre 2014;6(263):263ra158. ↩︎
- Braniste V, Al-Asmakh M, Kowal C, Anuar F, Abbaspour A, Tóth M, Korecka A, Bakocevic N, Ng LG, Kundu P, Gulyás B, Halldin C, Hultenby K, Nilsson H, Hebert H, Volpe BT, Diamond B, Pettersson S11. The gut microbiota influences blood-brain barrier permeability in mice. Sci Transl Med. 19 novembre 2014;6(263):263ra158. ↩︎
- Akkasheh G, Kashani-Poor Z & Tajabadi-Ebrahimi M et al (2016). Clinical and metabolic response to probiotic administration in patients with major depressive disorder: A randomized, double-blind, placebo-controlled trial. Nutrition. Vol 32. Issue 3. PP 315–20. ↩︎
- Zijlmans M, Korpela K & Riksen-Walraven JM (2015). Maternal prenatal stress is associated with the infant’s intestinal microbiota.Psychoneuroendocrinology. 53:233-45. ↩︎
- Messaoudi M, Violle N, & Bisson JF et al. (2011) Beneficial psychological effects of a probiotic formulation (Lactobacillus helveticus R0052 and Bifidobacterium longum R0175) in healthy human volunteers, Gut Microbes, 2:4, 256-261. ↩︎
- Matthew R. Hilimire, Jordan E. DeVylder, Catherine A. Forestell, Fermented foods, neuroticism, and social anxiety: An interaction model Psychiatry Research, 15 agosto 2015, Volume 228, Numero 2, pagine 203–208 ↩︎

